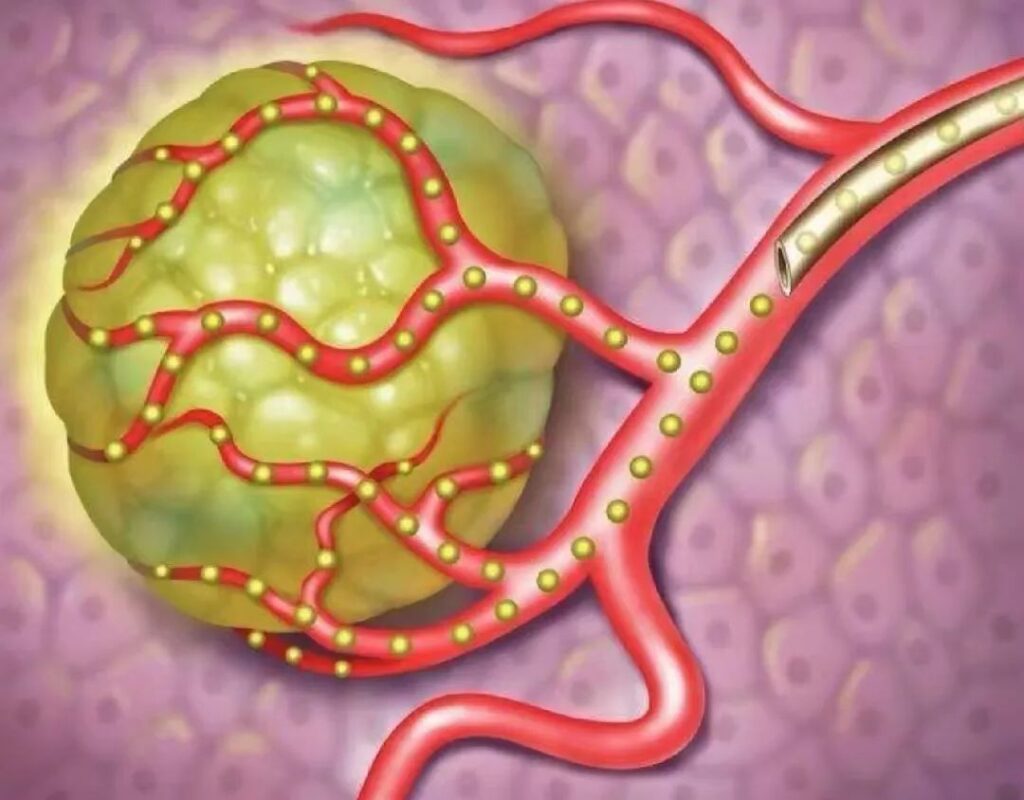
الكريات الدقيقة لتوصيل الأدوية تشير إلى جسيمات كروية تتشكل نتيجة إذابة أو تشتت الأدوية في مواد ذات مصفوفة بوليمرية، ويتراوح حجم جسيماتها عادةً بين 1 و250 ميكرومتر. ويمكن استخدامها في طرق إعطاء مختلفة، مثل الحقن الوريدي، والإعطاء الفموي، والإعطاء الموضعي عبر التجويف، أو الزرع تحت الجلد.
تُطلق تركيبات الكريات الدقيقة الأدوية ببطء، مما يُقلل من وتيرة الإعطاء، ويُقلل من تقلبات تركيز الدواء في الدم، ويُحقق تأثيرات علاجية طويلة الأمد. يُمكّن إدخال مواد مغناطيسية في الكريات الدقيقة أو تعديل المواد الحاملة لها من استهداف الآفات مغناطيسيًا أو بنشاط، وزيادة تركيز الدواء الفعال في الدم في الموقع المستهدف، وتقليل الآثار الجانبية السامة الجهازية للأدوية. يُمكن أن يُؤدي إدخال الكريات الدقيقة في شرايين الورم إلى قتل خلايا الورم من خلال العلاج بالانسداد، مما يُعيق تغذية الورم وإمداده بالدم أثناء إطلاق الأدوية، مما يزيد من التأثير العلاجي. بالإضافة إلى ذلك، تُخفي تركيبات الكريات الدقيقة أيضًا رائحة الأدوية الكريهة، وتُخفف من التهيج، وتُحسّن من ثبات الدواء.
وعلى وجه الخصوص، يمكن لأنظمة توصيل الأدوية باستخدام الكريات الدقيقة الاستفادة من مزاياها الخاصة لتحقيق التوصيل المحلي للأدوية ذات الجزيئات الكبيرة مثل الأدوية ذات الجزيئات الصغيرة والببتيدات والبروتينات والخلايا المعدلة وراثيا.
على سبيل المثال، يمكن للكرات الدقيقة أن تعزز التصاق وانتشار الخلايا الجذعية المتوسطة لنخاع العظم (BMSCs)، كما أن زرع الكرات الدقيقة في عيوب العظام يمكن أن يعزز تكوين العظام؛ عند استخدامها في الانصمام الكيميائي الشرياني عبر الشريان (TACE)، يمكن تحضير الكرات الدقيقة حسب الحاجة وفقًا لقطر الأوعية ومتطلبات العلاج لتحقيق تأثيرات الانصمام الأكثر دقة؛ تحضير الكرات الدقيقة في هياكل مسامية ومتعددة الطبقات، وتحميل محتويات مختلفة أثناء تشكيل خزان دواء طويل الأمد في الجسم الحي؛ الاستفادة من الاختلافات في معدلات تحلل المواد المختلفة لتحقيق إطلاق الدواء بشكل متسلسل أو تدريجي.
لقد حقق تطبيق مستحضرات الكريات الدقيقة في المجال الطبي تقدماً كبيراً، مع إطلاق العديد من المنتجات بنجاح، مما يوفر استراتيجيات علاجية مبتكرة لمختلف الأمراض.
1. طريقة تحضير الكريات الدقيقة لتوصيل الدواء
تتضمن عملية تحضير الكريات الدقيقة لتوصيل الدواء عادةً أربع خطوات: التشتيت، والتصلب، والغسل، والتجفيف. يشير التشتيت إلى التوزيع المنتظم للأدوية في مصفوفة بوليمرية من خلال الاستحلاب، والتحكم في ذوبان المذاب، وطرق أخرى لتشكيل هياكل الكريات الدقيقة. تتضمن عملية المعالجة تثبيت شكل وبنية الكريات الدقيقة من خلال طرق فيزيائية (مثل تبخير المذيبات، وتغيرات درجة الحرارة) أو طرق كيميائية (مثل تفاعلات الترابط)، ثم الغسل والتجفيف لإزالة الشوائب، مما ينتج عنه جسيمات كروية دقيقة قابلة للتخزين. تُصنف هذه المقالة الكريات الدقيقة المُحمّلة بالأدوية بناءً على طرق تحضير مختلفة، وتُحلل العمليات الأساسية لكل طريقة.

2.التطبيق السريري ل كرة مجهريةس توصيل الأدوية نظام
2.1 العلاج الموضعي للأورام الخبيثة
الأورام الخبيثة (السرطان) مرضٌ خطيرٌ يُهدد الاستقرار الاجتماعي والتنمية الاقتصادية في الصين. في عام 2022، من المتوقع أن تُسجل الصين حوالي 4.8 مليون حالة إصابة جديدة بالسرطان و2.5 مليون حالة وفاة بسببه. تشمل الأدوية المضادة للأورام المستخدمة حاليًا في الممارسة السريرية بشكل رئيسي الأدوية الموجهة جزيئيًا، وأدوية العلاج الكيميائي، وأدوية العلاج المناعي، والعلاج الخلوي. ولا يقتصر دور تغليف الأدوية المضادة للأورام في كريات مجهرية على تأخير معدل إطلاقها، والقضاء على خلايا الورم بشكل مستمر، والتغلب على مقاومة الأدوية وتواتر تناولها، بل يُقلل أيضًا من الآثار الجانبية من خلال استراتيجيات الإعطاء الموضعي أو الموضعي.
حضّر شي وآخرون كريات مجهرية من حمض البولي لاكتيك المسامي (PLA) بطريقة الغسول المزدوج وطريقة الاستخلاص بالمذيبات. باستخدام خصائص PLA ذاتية الشفاء، يُسبب تعريضه لأشعة تحت الحمراء الخفيفة ارتفاعًا في درجة الحرارة، مما يُحوّل PLA من حالة زجاجية إلى حالة مطاطية، ويُحفّز إعادة ترتيب سلاسل البوليمر تلقائيًا. تخضع هذه الكرات المجهرية المسامية لعملية شفاء، حيث تُحمّل جزيئات المستضد فيها لتحقيق تأثير إطلاق مُستدام.
يمكن للكرات المجهرية أيضًا تغليف عوامل تباين متنوعة للتصوير داخل الجسم الحي. جمع تشانغ وآخرون بين تقنيات الغزل الكهربائي والتجانس والرش الكهربائي لإعداد كرات مجهرية من الألياف محملة بالأدوية، مُعززة بحمض الهيالورونيك. يمكن لـ Gd3+ المُخلَّب على الكرات المجهرية تحقيق تصوير بالرنين المغناطيسي للأورام لمدة 5 أيام على الأقل.
لمنع النقائل والانتكاس بعد استئصال الورم الصلب، غالبًا ما يُستخدم العلاج المساعد، كالعلاج الكيميائي أو الإشعاعي، بعد الجراحة. ومع ذلك، فإن تركيز أدوية العلاج الكيميائي الذي يصل إلى العضو المستهدف بعد تناوله جهازيًا يكون محدودًا، ويتطلب الوصول إلى تركيز معين من الدواء جرعة أكبر، مما قد يؤدي إلى آثار جانبية سامة جهازية. استخدم تشونغ وآخرون طريقة الموائع الدقيقة وطريقة الرش الكهربائي لتحضير كريات مجهرية من ألجينات الكالسيوم تحتوي على كريات مجهرية متعددة من جيلاتين الميثاكريلول (GelMA).
تُملأ كريات ألجينات الكالسيوم المجهرية موضعيًا في موقع استئصال الورم. يؤدي التحلل السريع لكريات ألجينات الكالسيوم المجهرية إلى إطلاق سريع للدوكسوروبيسين للقضاء على خلايا الورم المتبقية، بينما تتحلل كريات جيلما المجهرية ببطء وبشكل مستمر، مما يُطلق مُحفز تجديد الكبد المُغلف. كما يمكن أن تعمل كريات جيلما المجهرية كسقالة لتجديد خلايا الكبد لتعزيز تجديدها.
في السنوات الأخيرة، حقق علاج الخلايا التائية مستقبلات المستضدات الكيمرية (CAR-T) استجابات سريرية فعالة وطويلة الأمد في علاج الأورام الخبيثة الدموية، ومن المتوقع أن يُحدث تغييرًا جذريًا في الوضع الراهن لعلاج سرطان الدم. إلا أن فعالية علاج الخلايا التائية مستقبلات المستضدات الكيمرية محدودة حاليًا في الأورام الصلبة، ويعود ذلك أساسًا إلى أن كثافة المصفوفة خارج الخلوية والجهاز الوعائي غير الطبيعي للأورام الصلبة يحدان من تسلل خلايا الخلايا التائية مستقبلات المستضدات الكيمرية إلى الورم.
مستوحى من العملية الفسيولوجية لتكاثر الخلايا التائية في العقد الليمفاوية، قام لياو وآخرون بإعداد هياكل اصطناعية للعقد الليمفاوية من الكريات الدقيقة PLGA باستخدام طريقة الميكروفلويديك لتحميل خلايا CAR-T وتغليف العديد من السيتوكينات، ومحاكاة جزيئات الإشارة الرئيسية التي توفرها الخلايا المقدمة للمستضد (APCs) لتنشيط الخلايا التائية.
2.2 يستخدم لعلاج أمراض العظام مثل إصلاح عيوب العظام
تتميز البيئة الدقيقة لإصابة العظام بالالتهاب والحموضة وارتفاع مستويات أنواع الأكسجين التفاعلية (ROS). تلعب أدوية مثل السيتوكينات دورًا حاسمًا في إصلاح عيوب العظام، إلا أن استخدامها محدود بسبب عدم قدرة السيتوكينات على الحفاظ على نشاطها طويل الأمد في بيئات الجسم المعقدة. توفر الكريات الدقيقة بيئة دقيقة مستقرة لها، مما يحافظ على نشاطها لفترة طويلة ويحقق تأثير إطلاق مستدام. كما أن قابلية حقن الكريات الدقيقة تسمح بزرعها في أجسام المرضى لملء مناطق عيوب العظام غير المنتظمة. قام سونغ وآخرون بتحميل جسيمات نانوية من ثاني أكسيد المنغنيز (MnO2) وبروتين تكوين العظام-2 (BMP-2) على الكريات الدقيقة PLGA. وقد تم تحقيق الإطلاق السريع للأدوية عند الطلب باستخدام تقنية الموجات فوق الصوتية منخفضة التردد.

على الرغم من أن أنسجة العظام تتمتع بقدرة تجديدية معينة، إلا أنه في حالات عيوب العظام الأكبر حجمًا والتي تتجاوز قدرتها على الشفاء الذاتي، عادةً ما يلزم زرع طُعم عظمي لتحقيق نتائج علاجية فعالة. حضّر هاو وآخرون كريات مجهرية من جل إم إيه/حمض الميثاكريلوئيل هيالورونيك (HAMA) تُغلّف مسحوق مصفوفة العظام المُزالة الكلس (DBM) وعامل نمو بطانة الأوعية الدموية باستخدام طريقة الموائع الدقيقة، ثم وضعوا الكريات المجهرية في هياكل مصفوفة العظام المُزالة الكلس (DBM) لزرعها في عيوب العظام.
بالمقارنة مع هيدروجيل الكتل، يمكن للخلايا المحمّلة على سطح الكريات الدقيقة أن تتلامس بشكل كامل مع المصفوفة خارج الخلية. كما تضمن مسام الكريات الدقيقة نفاذ العناصر الغذائية ونقلها. وفي الوقت نفسه، تُساعد المسام الموجودة بين الكريات الدقيقة على تكوين الأوعية الدموية، مما يُعزز بشكل فعال التصاق خلايا نخاع العظم الجذعية وانتشارها وتمايزها العظمي.
2.3 يستخدم لعلاج أمراض الجهاز العصبي المركزي مثل إصابة الحبل الشوكي
تشمل الإصابات العصبية إصابات الجهاز العصبي المركزي والطرفي، وكلاهما يُشكل تحديات في العلاج السريري والتعافي الوظيفي، وخاصةً تلك المتعلقة بالحبل الشوكي. يُسجل عالميًا ما يقارب 40 حالة إصابة بالحبل الشوكي لكل مليون شخص، وغالبًا ما تؤدي إصابة الحبل الشوكي، في حال عدم وجود علاج فعال، إلى إعاقة مدى الحياة. يُعد زرع الخلايا الجذعية العصبية في مواقع إصابة الحبل الشوكي حاليًا استراتيجية علاجية واعدة. ومع ذلك، نظرًا لتأثير البيئة المرضية، فإن معدل بقاء الخلايا المزروعة وكفاءة تمايزها منخفضان نسبيًا.
حضّر وو وآخرون كرةً مجهريةً من الببتيد تُحاكي عامل النمو المشتق من الصفائح الدموية (PDGF). تتكون هذه الكرة من خماسي الببتيد VRKKP، الموجود بين بقايا تسلسل PDGF من 159 إلى 163، وحمض النفثيل أسيتيك - فينيل ألانين - فينيل ألانين - جلايسين، وذلك لإنتاج كرات مجهرية من الهيدروجيل ذاتية التجميع. من بينها، يُمكن لخماسي الببتيد VRKKP محاكاة وظيفة PDGF، بما في ذلك منع موت الخلايا العصبية، وزيادة كفاءة تمايز الخلايا الجذعية العصبية، وما إلى ذلك، مما يُحسّن معدل بقاء زراعة الخلايا الجذعية العصبية، ويُحقق تأثيرات تآزرية.
2.4 لعلاج أمراض الجهاز التنفسي مثل عدوى فيروس كورونا الجديد
فيروس كورونا 2 المسبب لمتلازمة الجهاز التنفسي الحادة الوخيمة (SARS-CoV-2) هو فيروس شديد العدوى ومسبب للأمراض، ويسبب عدوى فيروس كورونا المستجد (كوفيد-19)، مسببًا التهابات تنفسية حادة. في الوقت الحالي، غالبًا ما تتطلب اللقاحات جرعات متعددة لتنشيط الجهاز المناعي بالكامل. يُحسّن نظام توصيل الأدوية المجهري استقرار الدواء وإطلاقه المستدام على المدى الطويل، ويمكنه تغليف بعض المواد المستجيبة، مثل جسيمات أكسيد الحديد النانوية، لاستهدافها بدقة، مما يُمكّن من توصيل اللقاحات إلى الخلايا المُقدّمة للمستضد بدقة، وتحقيق تأثيرات مناعية أفضل.
قام تشين وآخرون بتصنيع كريات جيلما المجهرية باستخدام تقنية الطباعة الحجرية بالليزر ثلاثية الأبعاد بتقنية البلمرة ثنائية الفوتون لتوصيل لقاح الحمض النووي (الشكل 3أ). يمكن تعديل مستوى الارتباط المتبادل بين الكريات المجهرية عن طريق تغيير قوة الليزر، مما يتحكم في إطلاق الأدوية. من خلال تصنيع كريات جيلما المجهرية على سقالة مغناطيسية، يمكن تحقيق قابلية التشغيل والاستهداف لتوصيل لقاحات الحمض النووي إلى الخلايا الشجيرية والخلايا الأولية، مما يقلل من التأثيرات غير المستهدفة ويحقق توصيلًا دقيقًا للقاح.
2.5 يستخدم لتنظيم ميكروبات الأمعاء
أظهرت الأبحاث أن ميكروبات الأمعاء تلعب دورًا هامًا في مرض التهاب الأمعاء، بل وفي الجهاز المناعي بأكمله. يمكن للبروبيوتيك الفموي علاج أمراض الجهاز الهضمي من خلال تنظيم ميكروبات الأمعاء. ومع ذلك، فإن الظروف البيئية للجهاز الهضمي (مثل وجود حمض المعدة وإنزيمات هضمية مختلفة) تؤدي إلى انخفاض معدلات البقاء على قيد الحياة وقلة استعمار البروبيوتيك الفموي، مما يحد بشكل كبير من استخدامها. قام يانغ وآخرون بإضافة ميثاكريلات إلى دكسترين وحمض التانيك (TA)، وخلطوا المحلولين، وجمّدوهما تحت الضوء المرئي (405 نانومتر).
استُخدمت الكريات الدقيقة الهيدروجيلية المُحضرة لتغليف بكتيريا الإشريكية القولونية Nissle1917 وحمض الإندول-3-بروبيونيك (الشكل 4). تجمع هذه الكريات الدقيقة بين استقرار البكتين في المعدة والأمعاء الدقيقة وخصائص التصاق حمض التولوين الغني بمجموعات الكاتيكول في الأمعاء. يمكن أن يُقلل استخدام هذه الكريات الدقيقة في نموذج التهاب القولون لدى الفئران من التهاب الأمعاء ويُعيد وظيفة الحاجز المعوي.
الخاتمة والتوقعات
تُلخّص هذه المقالة بشكلٍ منهجي طرق تحضير وتطبيقات أنظمة توصيل الأدوية باستخدام الكريات الدقيقة، وتناقش التحديات التي تواجه التطبيق السريري لهذه الأنظمة الحديثة. على الرغم من أن الطرق الحالية لتحضير الكريات الدقيقة المُحمّلة بالأدوية، مثل تبخير مذيب المستحلب وفصل الطور، لها عيوبٌ مثل التوزيع غير المتساوي لحجم الجسيمات واستخدام كميات كبيرة من المذيبات العضوية، إلا أنها تتميز بمزايا من حيث التكلفة، وهي أكثر ملاءمةً للإنتاج على نطاق واسع.
أصبحت طرق استحلاب الأغشية، وطريقة الموائع الدقيقة، وطريقة الموائع فوق الحرجة، وغيرها، تدريجيًا مجالات بحثية واعدة نظرًا لمزاياها المتمثلة في حجم الجسيمات الموحد، والتوزيع المتحكم فيه، والمحافظة على البيئة. للحصول على كريات دقيقة محملة بالأدوية ذات أداء أفضل أو لتلبية متطلبات تطبيقات محددة، يمكن الجمع بين تقنيات مختلفة لتحضير الكرات الدقيقة.
في حالات مختلفة، يمكن الجمع بين مزايا الكريات الدقيقة والخصائص المرضية للأمراض لتحسين عيوب الأدوية الحالية. عادةً ما تُحمّل الكريات الدقيقة أدوية متعددة، مستفيدةً من خصائص بنيتها لتحقيق استراتيجيات إطلاق متنوعة، مثل تزامن وتدرج الأدوية المختلفة. في الوقت نفسه، يمكن دمج الكريات الدقيقة مع حاملات هياكل أخرى، مثل هيدروجيل الكتل، وسقالة تجديد العظام (مصفوفة العظام منزوعة الكلس)، لتعويض القوة الميكانيكية لكل منها وكفاءة بذر الخلايا، أو تعديل المواد المُحضرة لإضافة خصائص جديدة، مثل تعديل Gd3+ على مواد الكريات الدقيقة لتحقيق تصوير الورم.

على الرغم من أن الترجمة السريرية لأنظمة توصيل الأدوية الدقيقة تواجه العديد من التحديات، مثل صعوبة التحكم بدقة في معدلات إطلاق الدواء ونقص المعدات القياسية، فإن التعاون متعدد التخصصات في الصيدلة وعلوم المواد وغيرها من المجالات يمكن أن يحل بشكل مشترك الصعوبات في عملية تضخيم تقنية توصيل الأدوية الدقيقة وتحسين عملية تحضير الأدوية الدقيقة بشكل مستمر، مما يمكن أن يسرع تطوير وتحويل أنظمة توصيل الأدوية الدقيقة.
مع تعمق البحث والتقدم التكنولوجي، من المتوقع أن يقوم مطورو الأدوية بتصميم وتطوير منتجات كريات دقيقة لتوصيل الأدوية ذات تأثيرات إطلاق مستدامة/محكومة أفضل وعمليات إنتاج أكثر اكتمالاً.