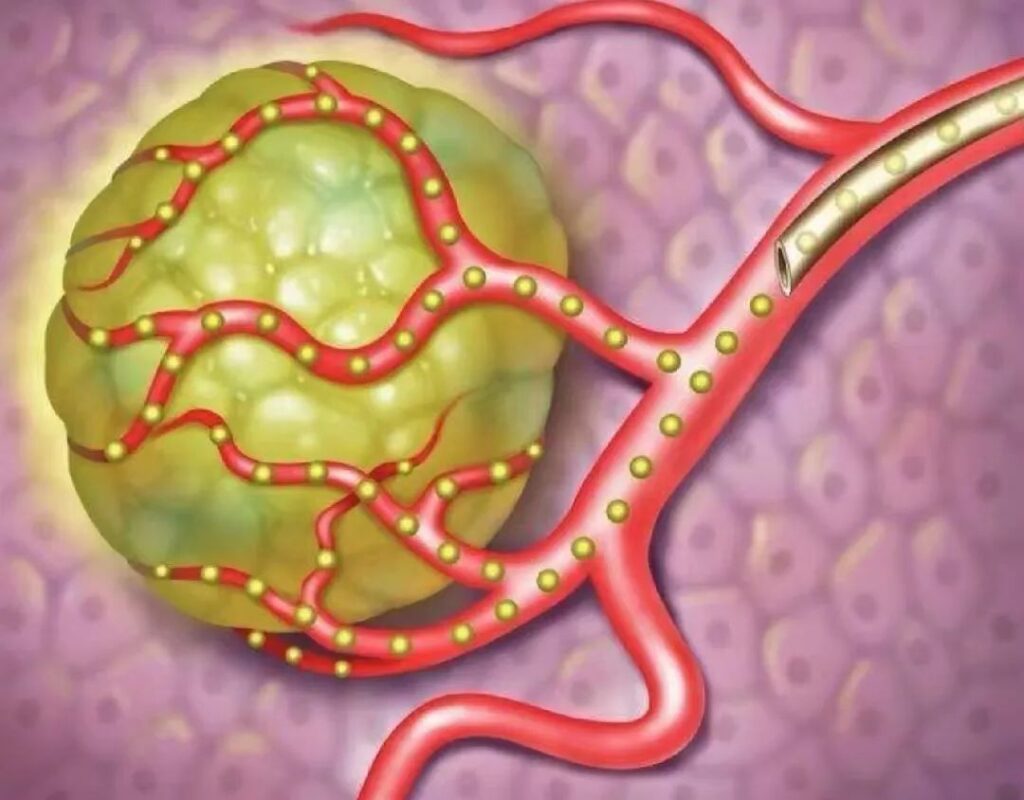
Микросферы для доставки лекарств относятся к сферическим частицам, образованным путем растворения или дисперсии лекарственных средств в полимерных матричных материалах, с размером частиц, как правило, от 1 до 250 мкм. Они могут использоваться для различных путей введения, таких как внутривенная инъекция, пероральное введение, местное введение через полость или подкожная имплантация.
Составы микросфер могут медленно высвобождать лекарственные средства, тем самым уменьшая частоту введения, снижая колебания концентрации лекарственных средств в крови и оказывая долгосрочное терапевтическое воздействие. Введение магнитных веществ в микросферы или модификация материалов-носителей может позволить микросферам магнитно или активно нацеливаться на поражения, увеличивать эффективную концентрацию лекарственных средств в крови в целевом месте и уменьшать системные токсические побочные эффекты лекарственных средств. Введение микросфер в артерии опухоли может убивать опухолевые клетки посредством эмболизационной терапии, блокируя питание и кровоснабжение опухоли при высвобождении лекарственных средств, что еще больше увеличивает терапевтический эффект. Кроме того, составы микросфер могут также маскировать неприятный запах лекарственных средств, уменьшать раздражение и улучшать стабильность лекарственных средств.
В частности, системы доставки лекарств на основе микросфер могут использовать свои собственные преимущества для обеспечения локальной доставки крупномолекулярных препаратов, таких как низкомолекулярные препараты, пептиды, белки и сконструированные клетки.
Например, микросферы могут способствовать адгезии и пролиферации мезенхимальных стволовых клеток костного мозга (BMSC), а имплантация микросфер в дефекты костей может способствовать формированию костной ткани; При использовании для трансартериальной химиоэмболизации (TACE) микросферы можно готовить по мере необходимости в соответствии с диаметром сосуда и требованиями к лечению для достижения более точного эффекта эмболизации; Подготавливать микросферы в пористых и многослойных структурах, загружая различное содержимое, при этом формируя длительный резервуар лекарственного средства in vivo; Использовать различия в скорости деградации различных материалов для достижения последовательного или градиентного высвобождения лекарственного средства.
Применение препаратов на основе микросфер в медицинской сфере достигло значительного прогресса: на рынок успешно выведено множество продуктов, предлагающих инновационные стратегии лечения различных заболеваний.
1. Метод приготовления микросфер для доставки лекарственных средств
Процесс приготовления микросфер для доставки лекарств обычно включает четыре этапа: дисперсию, затвердевание, промывку и сушку. Дисперсия относится к равномерному распределению лекарств в полимерной матрице посредством эмульгирования, контроля растворимости растворенного вещества и других методов для формирования структур микросфер. Отверждение включает фиксацию морфологии и структуры микросфер с помощью физических методов (таких как испарение растворителя, изменение температуры) или химических методов (таких как реакции сшивания), а затем промывку и сушку для удаления примесей, в результате чего получаются частицы микросфер, которые можно хранить. В этой статье классифицируются микросферы, загруженные лекарствами, на основе различных методов приготовления, анализируются основные процессы каждого метода.

2.Клиническое применение Микросферас Доставка лекарств Система
2.1 Местное лечение злокачественных опухолей
Злокачественные опухоли (рак) являются серьезным заболеванием, которое угрожает социальной стабильности и экономическому развитию в Китае. В 2022 году в Китае будет около 4,8 миллиона новых случаев рака и 2,5 миллиона смертей от рака. Противоопухолевые препараты, которые в настоящее время используются в клинической практике, в основном включают молекулярные таргетные препараты, химиотерапевтические препараты, иммунотерапевтические препараты и клеточную терапию. Инкапсуляция противоопухолевых препаратов в микросферы может не только замедлить скорость высвобождения, непрерывно убивать опухолевые клетки, преодолеть возникновение лекарственной устойчивости и частоту введения, но и уменьшить побочные реакции с помощью стратегий местного или in situ введения.
Си и др. подготовили пористые микросферы полимолочной кислоты (PLA) методом двойного лосьона и методом экстракции растворителем. Используя самовосстанавливающиеся свойства PLA, мягкое инфракрасное облучение вызывает повышение температуры, преобразуя PLA из стекловидного состояния в резиноподобное состояние и запуская спонтанную перестройку полимерных цепей. Эта пористая микросфера будет подвергаться заживлению, загружая молекулы антигена в микросферу для достижения эффекта пролонгированного высвобождения.
Микросферы также могут инкапсулировать различные контрастные агенты для визуализации in vivo. Чжан и др. объединили электропрядение, гомогенизацию и технологию электрического распыления для приготовления волокнистых микросфер с функционализированным гиалуроновой кислотой, загруженных лекарственным средством. Хелатированный на микросферах Gd3+ может обеспечить магнитно-резонансную томографию опухолей в течение как минимум 5 дней.
Для предотвращения метастазов и рецидива после резекции солидной опухоли часто применяется послеоперационная адъювантная терапия, такая как химиотерапия или радиотерапия. Однако концентрация химиотерапевтических препаратов, достигающая целевого органа после системного введения, ограничена, а достижение определенной концентрации препарата требует большей дозы, что может привести к системным токсическим побочным эффектам. Чжун и др. использовали микрофлюидный метод и метод электрического распыления для приготовления микросфер альгината кальция, содержащих несколько микросфер метакрилоилжелатина (GelMA).
Микросферы альгината кальция заполняются in situ в месте резекции опухоли. Быстрая деградация микросфер альгината кальция приводит к быстрому высвобождению доксорубицина для уничтожения остаточных опухолевых клеток, в то время как микросферы GelMA медленно деградируют и непрерывно высвобождают инкапсулированный стимулятор регенерации печени. Микросферы GelMA также могут служить каркасом для регенерации клеток печени, способствуя регенерации печени.
В последние годы терапия химерными антигенными рецепторами Т-клеток (CAR-T) дала эффективные и долгосрочные клинические ответы при лечении гематологических злокачественных новообразований и, как ожидается, изменит текущий статус лечения гематологического рака. Однако в настоящее время терапия CAR-T имеет ограниченную эффективность в солидных опухолях, в основном потому, что плотный внеклеточный матрикс и аномальная сосудистая система солидных опухолей ограничивают инфильтрацию опухоли CAR-T-клетками.
Вдохновленные физиологическим процессом пролиферации Т-клеток в лимфатических узлах, Ляо и соавторы подготовили искусственные каркасы лимфатических узлов из микросфер PLGA, используя микрофлюидный метод для загрузки CAR-T-клеток и инкапсуляции множественных цитокинов, имитируя ключевые сигнальные молекулы, предоставляемые антигенпрезентирующими клетками (АПК) для активации Т-клеток.
2.2 Используется для лечения ортопедических заболеваний, таких как восстановление дефектов костей.
Микросреда костной травмы характеризуется воспалением, кислотностью и высокой экспрессией активных форм кислорода (ROS). Такие препараты, как цитокины, играют решающую роль в восстановлении костных дефектов, но их применение ограничено неспособностью цитокинов поддерживать длительную активность в сложных средах организма. Микросферы могут обеспечить для него стабильную микросреду, которая может сохранять свою активность в течение длительного времени и достигать эффекта пролонгированного высвобождения. А инъекционная способность микросфер позволяет имплантировать их в тела пациентов для заполнения нерегулярных областей костных дефектов. Song et al. загрузили наночастицы диоксида марганца (MnO2) и костный морфогенетический белок-2 (BMP-2) на микросферы PLGA. Оперативное высвобождение лекарств по требованию было достигнуто с помощью низкочастотной ультразвуковой технологии.

Хотя костная ткань обладает определенной регенеративной способностью, для более крупных дефектов костей, которые превышают способность костной ткани к самовосстановлению, для достижения эффективных результатов лечения обычно требуется имплантация костного трансплантата. Хао и др. подготовили микросферы GelMA/метакрилоилгиалуроновой кислоты (HAMA), инкапсулирующие порошок декальцинированного костного матрикса (DBM) и фактор роста эндотелия сосудов, с помощью микрофлюидного метода и загрузили микросферы в каркасы DBM для имплантации в дефекты костей.
По сравнению с блочным гидрогелем, клетки, загруженные на поверхность микросфер, могут полностью контактировать с внеклеточным матриксом. Поры микросфер также обеспечивают проникновение и транспортировку питательных веществ. В то же время поры между микросферами способствуют образованию кровеносных сосудов, что может эффективно способствовать адгезии, пролиферации и остеогенной дифференцировке BMSC.
2.3 Используется для лечения заболеваний центральной нервной системы, таких как повреждение спинного мозга.
Неврологические травмы включают травмы центральной нервной системы и травмы периферической нервной системы, обе из которых создают проблемы в клиническом лечении и функциональном восстановлении, особенно те, которые связаны со спинным мозгом. Во всем мире насчитывается около 40 случаев травмы спинного мозга (SCI) на миллион человек, и без эффективного лечения травма спинного мозга часто приводит к пожизненной инвалидности. В настоящее время трансплантация нейральных стволовых клеток (NSC) в области SCI считается многообещающей терапевтической стратегией. Однако из-за влияния патологической микросреды выживаемость и эффективность дифференциации трансплантированных клеток относительно низкие.
Ву и др. подготовили микросферу пептида, имитирующего тромбоцитарный фактор роста (PDGF). Микросфера состоит из пентапептида VRKKP между остатками последовательности PDGF 159~163 и нафтилуксусной кислоты – фенилаланина – фенилаланина – глицина для создания самоорганизующихся гидрогелевых микросфер. Среди них пентапептид VRKKP может имитировать функцию PDGF, включая предотвращение гибели нейронов, повышение эффективности дифференциации НСК и т. д., тем самым улучшая выживаемость трансплантированных НСК и оказывая синергетический эффект.
2.4 Для лечения респираторных заболеваний, таких как новая коронавирусная инфекция
Тяжелый острый респираторный синдром коронавируса 2 (SARS-CoV-2) является высокоинфекционным и патогенным вирусом, который вызывает новую коронавирусную инфекцию (коронавирусное заболевание 2019, COVID-19), вызывающую острые респираторные инфекции. В настоящее время вакцины часто требуют многократных доз для полной активации иммунной системы. Система доставки лекарств с микросферами имеет эффект улучшения стабильности лекарств и длительного замедленного высвобождения лекарств и может инкапсулировать некоторые чувствительные материалы, такие как наночастицы оксида железа, для нацеливания, что может точно доставлять вакцины к АПК и достигать лучших иммунных эффектов.
Чен и др. изготовили микросферы GelMA с использованием технологии двухфотонной полимеризации 3D лазерной литографии для доставки ДНК-вакцины (рисунок 3A). Изменение мощности лазера может регулировать уровень сшивания микросфер, тем самым контролируя высвобождение лекарств. Изготавливая микросферы GelMA на магнитном каркасе, можно добиться работоспособности и нацеливания для доставки ДНК-вакцин в дендритные клетки и первичные клетки, уменьшая нецелевые эффекты и достигая целевой доставки вакцины.
2.5 Используется для регуляции микробиоты кишечника
Исследования показали, что микробиота кишечника играет важную роль в воспалительных заболеваниях кишечника и даже в работе всей иммунной системы. Оральные пробиотики могут лечить желудочно-кишечные заболевания, регулируя микробиоту кишечника. Однако условия желудочно-кишечной среды (такие как наличие желудочной кислоты и различных пищеварительных ферментов) приводят к низкой выживаемости и недостаточной колонизации оральных пробиотиков, что значительно ограничивает их применение. Янг и др. ввели метакрилат в декстран и дубильную кислоту (ТА), смешали два раствора и затвердели под видимым светом (405 нм).
Полученные гидрогелевые микросферы были использованы для инкапсуляции E. coli Nissle1917 и индол-3-пропионовой кислоты (рисунок 4). Эта микросфера сочетает в себе стабильность пектина в желудке и тонком кишечнике с адгезивными свойствами ТА, богатой катехольными группами в кишечнике. Использование этой микросферы в мышиной модели колита может уменьшить воспаление кишечника и восстановить барьерную функцию кишечника.
Заключение и перспективы
В этой статье систематически суммируются методы приготовления и клиническое применение систем доставки лекарств на основе микросфер, а также обсуждаются проблемы клинического перевода новых систем доставки лекарств на основе микросфер. Хотя существующие методы приготовления микросфер, загруженных лекарствами, такие как испарение растворителя эмульсии и разделение фаз, имеют недостатки, такие как неравномерное распределение размера частиц и использование больших количеств органических растворителей, они имеют преимущества в плане стоимости и больше подходят для крупномасштабного производства.
Метод мембранной эмульсификации, микрофлюидный метод, метод сверхкритической жидкости и т. д. постепенно стали горячими точками исследований благодаря своим преимуществам однородного размера частиц, контролируемого распределения и экологичности. Для получения микросфер, загруженных лекарственными средствами, с лучшими характеристиками или для соответствия конкретным требованиям применения можно комбинировать различные методы подготовки микросфер.
Для различных показаний преимущества микросфер и патологические характеристики заболеваний могут быть объединены для устранения недостатков существующих лекарств. Микросферы обычно могут загружать несколько лекарств, используя характеристики структуры микросфер для достижения различных стратегий высвобождения, таких как синхронизация и градиент различных лекарств. В то же время микросферы также могут быть объединены с носителями других структур, такими как блок-гидрогель, каркас регенерации кости (декальцинированный костный матрикс), чтобы компенсировать механическую прочность друг друга и эффективность засевания клеток, или модифицировать подготовленные материалы для введения новых свойств, таких как модифицированный Gd3+ на материалах микросфер для достижения визуализации опухоли.

Хотя клиническое применение систем доставки лекарств на основе микросфер сталкивается со многими трудностями, такими как сложность точного контроля скорости высвобождения лекарств и отсутствие стандартизированного оборудования, междисциплинарное сотрудничество в фармацевтике, материаловедении и других областях может совместно решить трудности в процессе амплификации технологии доставки лекарств на основе микросфер и постоянно оптимизировать процесс приготовления микросфер доставки лекарств, что может ускорить разработку и трансформацию систем доставки лекарств на основе микросфер.
Ожидается, что с углублением исследований и технологического прогресса разработчики лекарственных препаратов будут проектировать и разрабатывать продукты на основе микросфер для доставки лекарственных средств с улучшенными эффектами замедленного/контролируемого высвобождения и более полными производственными процессами.